 联系我们
联系我们
 18210828691
18210828691


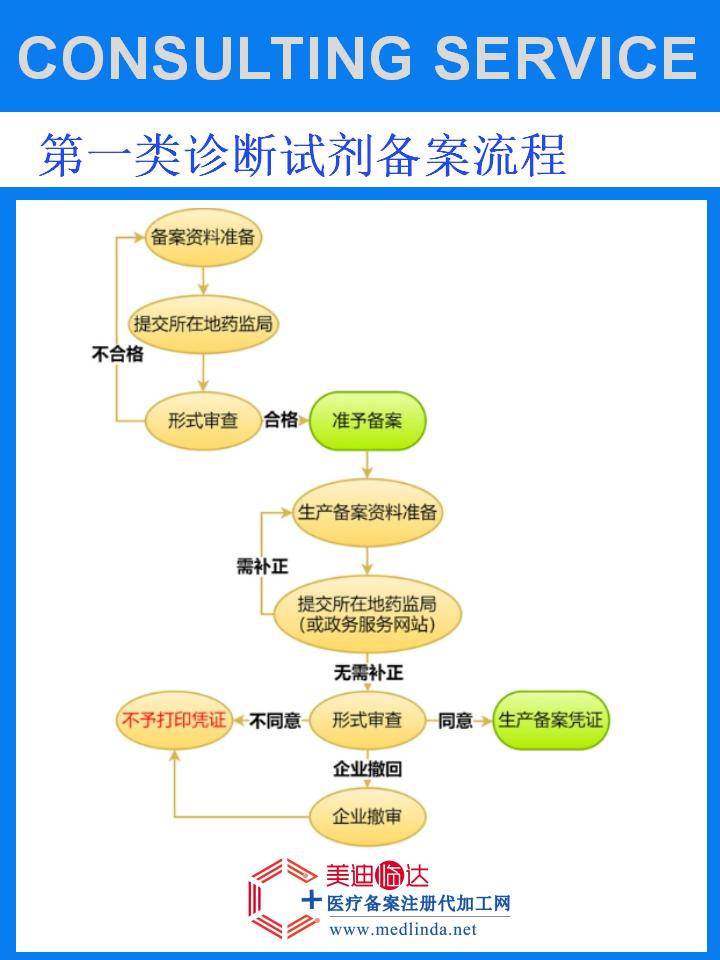





【图文】办理蛋白胨水培养基诊断试剂备案批准文号:解锁合规新高度,助力精准医疗
在微生物学研究与临床检验的精密舞台上,蛋白胨水培养基作为一种基础而关键的培养基,其重要性不言而喻。它以其独特的营养成分,为微生物的增殖与鉴定提供了理想的生长环境。随着#热门话题“医疗器械监管深化”的推进,办理蛋白胨水培养基诊断试剂的备案批准文号成为了企业确保产品合规上市、提升市场竞争力的重要一环。本文将为您详细解析办理流程,助您轻松解锁合规新高度,助力精准医疗的发展。
在医疗器械行业快速发展的今天,合规性已成为企业生存与发展的生命线。对于蛋白胨水培养基诊断试剂而言,获得备案批准文号不仅是法律法规的硬性要求,更是企业信誉与产品质量的体现。本文将为您提供一份详尽的备案批准文号办理指南,帮助您高效、顺利地完成这一关键步骤。
政策学习与准备:
首先,深入研读国家关于医疗器械备案及批准文号管理的政策法规,明确办理流程、所需材料及注意事项。同时,准备好企业资质证明、产品说明书、生产工艺流程、质量控制标准、检测报告等关键材料。
在线申报:
通过国家药品监督管理局指定的医疗器械注册管理信息系统进行在线申报。在申报过程中,需仔细填写企业信息、产品信息及备案申请表,并上传准备好的材料。注意信息的准确性和规范性,避免因信息错误导致审核延误。
资料审核:
提交申请后,监管部门将对申报材料进行严格审核。审核内容包括企业资质、产品质量、生产工艺等多个方面。企业需保持与监管部门的沟通联系,及时解答疑问并提供补充材料。
现场核查(如需要):
对于部分高风险或特殊产品,监管部门可能会组织现场核查。核查内容包括生产现场、质量管理体系、生产设备等。企业应提前做好准备工作,确保核查顺利进行。
审批与发证:
经过资料审核和(如需)现场核查后,监管部门将对申请进行审批。审批通过后,将颁发备案批准文号及备案凭证。这标志着产品已正式获得合法上市资格。
办理蛋白胨水培养基诊断试剂备案批准文号是企业合规化发展的重要一步。通过精心准备、严格审核及持续优化,您将能够顺利获得备案批准文号,为产品的市场准入奠定坚实基础。让我们携手并进,在精准医疗的广阔领域中共同创造更加辉煌的未来!