 联系我们
联系我们
 18210828691
18210828691


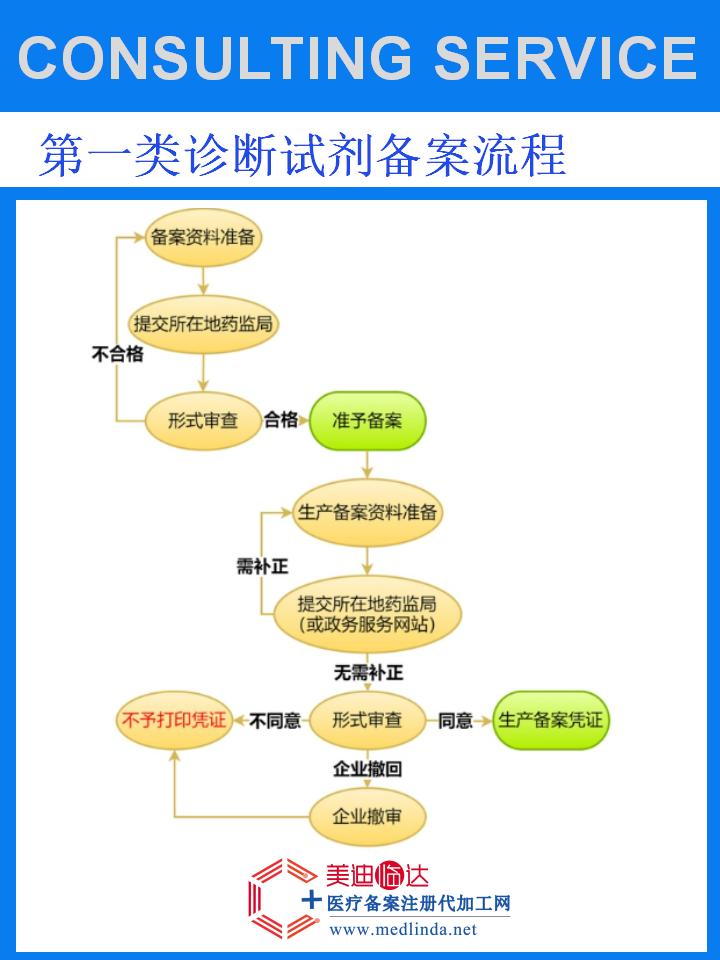





【图文】办理大豆酪蛋白琼脂(TSA)培养基诊断试剂(Ⅰ类)备案攻略:轻松解锁合规之门
在微生物学研究与临床诊断的精密领域,大豆酪蛋白琼脂(TSA)培养基以其均衡的营养成分和广泛的适用性,成为了细菌培养与鉴定的基石。随着#热门话题“医疗器械合规性强化”的兴起,办理大豆酪蛋白琼脂(TSA)培养基诊断试剂(Ⅰ类)备案成为了企业必须跨越的重要一步。本文将为您详细解析备案攻略,助您轻松解锁合规之门。
在医疗器械行业日益规范化的今天,合规性已成为企业生存与发展的基石。对于大豆酪蛋白琼脂(TSA)培养基诊断试剂(Ⅰ类)而言,完成备案不仅是法律法规的硬性要求,更是企业信誉与产品质量的象征。本文将为您提供一份详尽的备案攻略,帮助您高效、顺利地完成备案流程。
政策研读:首先,深入了解国家关于医疗器械备案的政策法规,特别是针对Ⅰ类医疗器械的具体要求。明确备案的适用范围、条件、流程及所需材料。
资料整理:根据备案要求,提前准备企业资质证明、产品说明书、生产工艺流程图、质量控制标准、检测报告等必要材料。确保所有资料真实、准确、完整,符合法规要求。
内部审核:在提交备案申请前,企业内部应进行严格的审核,确保产品质量管理体系健全有效,生产工艺符合规范要求,产品性能稳定可靠。
在线申报:通过国家药品监督管理局指定的医疗器械注册管理信息系统进行在线申报,填写相关信息并上传所需材料。注意信息的准确性和规范性,避免因信息错误导致审核延误。
资料审核:监管部门将对提交的备案申请进行资料审核,检查材料的完整性、真实性及合规性。企业需保持与监管部门的沟通联系,及时解答疑问并提供补充材料。
现场核查(如需要):对于部分高风险或特殊产品,监管部门可能会组织现场核查,以验证企业的生产条件、质量管理体系及产品质量是否符合要求。企业应积极配合核查工作,确保核查顺利进行。
公示与发证:审核通过后,监管部门将在官方平台上进行公示。公示期满后,企业将获得备案凭证及备案编号,标志着产品已正式获得合法上市资格。
办理大豆酪蛋白琼脂(TSA)培养基诊断试剂(Ⅰ类)备案是企业迈向合规化、品牌化发展的重要一步。通过精心准备、严格审核、积极配合及持续优化,您将能够顺利解锁合规之门,为产品的市场准入奠定坚实基础。让我们携手并进,在微生物学研究与临床诊断的广阔领域中共同创造更加辉煌的未来!